Для врачей
Показания к инвазивным методам лечения фибрилляции предсердий
Фибрилляция предсердий (ФП) – самое распространённое нарушение ритма сердца, представляющее собой хаотичное возбуждение предсердий, с нерегулярным проведением импульса на желудочки сердца. ФП составляет более 40% среди всех видов нарушений ритма.
Причины возникновения его различны. ФП может возникать у людей без органических заболеваний сердца, идиопатическая ФП, после перенесенного миокардита или у больных с ишемической болезнью сердца на фоне явлений кардиосклероза, при острых интоксикациях, например алкоголем, синдром «праздничного сердца», довольно распространённое явление. Морфологическим субстратом ФП является миокард левого предсердия, который является таковым в силу особенностей строения и своей иннервации.
По характеру течения разделяют впервые возникшую – впервые зарегистрированную вне зависимости от продолжительности пароксизма; пароксизмальную форму ФП, характеризующуюся рецидивирующим течением (не менее 2-х эпизодов) со спонтанным восстановлением синусового ритма в течение 7 суток или восстановлением синусового ритма методом кардиоверсии в течение 48 часов; персистирующую – более 7 суток, купирующуюся приёмом медикаментов или электрической кардиоверсией после 48 часов от начала пароксизма; длительно существующую персистирующую, длящуюся более 1 года; постоянную – если пациентом и лечащим врачом принимается решение об отказе от восстановления ритма и сохранение аритмии считается приемлемым.
Пациенты чаще всего жалуются на нерегулярное сердцебиение, общую слабость, чувство нехватки воздуха, головокружение, иногда, обмороки. При объективном осмотре выслушиваются неритмичные частые тоны сердца, частота которых выше частоты пульса, так называемый феномен «дефицита пульса». На ЭКГ отмечается при неритмичной желудочковой активности отсутствие предшествующая ей предсердная волна «Р»; предсердная активность представлена хаотичными волнами «F».
Лечение, как правило, начинается с применения антиаритмических препаратов. При отсутствии органической патологии сердца, ИБС, препаратами первой линии являются антиаритмики I группы по классификации Vaughan-Williams, Пропафенон и Этацизин, которые принимаются пациентом по необходимости, при возникновении пароксизма ФП, «таблетка в кармане». При отсутствии эффекта или при наличии ИБС назначаются препараты III группы, Соталол, Амиодарон. Все пациенты с любой формой ФП нуждаются в приёме дезагрегантов (Аспирин не менее 100 мг в сутки) или антикоагулянтов (Варфарин 2,5 – 5 мг в сутки) под обязательным контролем МНО (2 – 2,5 – 3). С целью восстановления синусового ритма применяется медикаментозная (Новокаинамид, Амиодарон) либо электрическая, в т. ч. и низкоэнергетическая эндокардиальная (внутрисердечная), кардиоверсия. Всем пациентам имеющим ФП более 48 часов показана чреспищеводная эхокардиография для исключения наличия тромба в ЛП и антикоагулянтная подготовка.
В 2007 г. впервые был опубликован консенсусный документ с рекомендациями по показаниям к катетерным и хирургическим методам лечения фибрилляции предсердий при сотрудничестве организаций Heart Rhythm Society (HRS), European Heart Rhythm Association (EHRA), European Cardiac Arrhythmia Society (ECAS), Society of Thoracic Surgeon (STS), American College of Cardiology (ACC). За последнее десятилетие инвазивные методы лечения ФП стремительно развивались и росло количество клиник во всём мире, в которых они применялись.
Класс I рекомендаций означает, что выгоды от процедура абляции ФП значительно превышают риски, и что абляция ФП должна быть выполнены. Рекомендации класса IIa означает, что польза от аблации ФП превышают риски, и что это разумно её выполнение. Рекомендация Класс IIb означает, что клиническая выгода от абляции ФП больше или равна рискам, и что выполнение абляции ФП может быть рассмотрено. Рекомендация III класса означает, что ФП абляции не имеет доказанной эффективности и не рекомендуется. Если данные получены из нескольких рандомизированных клинических исследований или мета-анализов (отдельных исследований) или отдельных мета-анализов, это соответствует уровню доказательства А. Уровень доказательств B, когда данные были получены из одного рандомизированного исследования или нескольких нерандомизированных исследований. Уровень доказательств C, когда первичный источником рекомендаций являлся консенсус мнений, исследования клинических ситуаций или стандарты медицинской помощи.
Последний консенсус экспертов, представляющих семь организаций: Американский колледж кардиологов (ACC), Американская ассоциация сердца (AHA), Общество сердечного ритма Азиатско-Тихоокеанского региона (APHRS), Европейское общество аритмий сердца (ECAS), Европейская ассоциация ритма сердца (EHRA), Общества торакальных хирургов (STS), Североамериканское общество ритма сердца (HRS), был опубликован в 2012 г. Создание этот документа было основано на предыдущем варианте, а так же на накопленном опыте и новых данным, полученных от различных исследований, имеющих различный уровень доказательств.
В 2007 году согласно HRS/EHRA/ESC консенсусу экспертов по катетерной аблации и хирургическому лечению фибрилляции предсердий определяется, что основным показанием для катетерной аблации ФП является наличие симптомной ФП, рефрактерной или толерантной по крайней мере к одному антиаритмическому препарату класса I или III по классификации Vaughan-Williams. В 2007 году экспертная группа также признала, что в редких клинические ситуации, может быть целесообразно для выполнения катетера абляции ФП качестве первой линии терапии. С момента публикации этого документа прошло пять лет, большое количество исследований, в том числе нескольких рандомизированных клинических исследований1,2, накоплен огромный опыт, который подтверждает безопасность и эффективность катетерной аблации ФП. Более того, пятилетнее наблюдение доказывает преимущество катетерной аблации перед медикаментозной терапии по части удержания синусового ритма и по количеству негативных явлений.
Согласно консенсусу экспертов HRS/EHRA/ESC 2012 года при симптомной пароксизмальной форме фибрилляции предсердий, устойчивой по крайней мере к одному антиаритмическому препарату класса I или III, рекомендована катетерная аблация, класс показаний I, уровень доказательств А; выполнение хирургической аблации этой группе пациентов будет иметь смысл при наличии других показаний к открытой операции на сердце, класс показаний IIА, уровень доказательств С. При персистирующей форме ФП имеет смысл выполнение катетерной аблации, класс показаний IIА, уровень доказательств В; выполнение хирургической аблации этой группе пациентов будет иметь смысл при наличии других показаний к открытой операции на сердце, класс показаний IIА, уровень доказательств С. При длительно существующей персистирующей форме ФП возможно выполнение катетерной аблации, класс показаний IIА, уровень доказательств В; выполнение хирургической аблации этой группе пациентов будет иметь смысл при наличии других показаний к открытой операции на сердце, класс показаний IIА, уровень доказательств С.
При симптомной пароксизмальной форме фибрилляции предсердий выполнения катетера абляции в качестве первой линии лечения, до назначения антиаритмических препаратов, имеет смысл, класс показаний IIА, уровень доказательств В; выполнение хирургической аблации этой группе пациентов будет иметь смысл при наличии других показаний к открытой операции на сердце, класс показаний IIА, уровень доказательств С. При нелеченой персистирующей форме ФП выполнение катетерной аблации может быть рассмотрено, класс показаний IIВ, уровень доказательств С; выполнение хирургической аблации этой группе пациентов будет иметь смысл при наличии других показаний к открытой операции на сердце, класс показаний IIА, уровень доказательств С. При длительно существующей персистирующей форме ФП возможно выполнение катетерной аблации до назначения антиаритмиков, класс показаний IIВ, уровень доказательств С; выполнение хирургической аблации этой группе пациентов может быть рассмотрена при наличии других показаний к открытой операции на сердце, класс показаний IIВ, уровень доказательств С.
Основным видом хирургии ФП является миниинвазивная операция, эндокардиальная катетерная радиочастотная деструкция (аблация, РЧА) в левом предсердии, направленная на денервацию ЛП, сокращение критической массы фибриллирующего миокарда и изоляция очагов, чаще всего располагающихся в устьях лёгочных вен. Эффективность данного вида лечения достигает 70-85%, при этом необходимость в повторном вмешательстве составляет около 30%. Различные осложнения возникают у менее 5% пациентов. Во всём Мире эта операция является методом выбора у пациентов с пароксизмальной и персистирующей ФП. Противопоказанием к данной операции является наличие тромба в ушке ЛП. Краткое описание техники катетерной РЧА: трансвенозным доступом устанавливаются электроды в коронарный синус и для РЧА, выполняется пункция межпредсердной перегородки, для определения конечной точки, достижения критериев электрической изоляции лёгочных вен от тела ЛП, используется циркулярный диагностический катетер, который устанавливается в устье лёгочных вен типа Lasso. Под контролем специального оборудования, электрофизиологической станции с эндокардиальными отведениями и навигационной станции, выполняется электроанатомическое картирование левого предсердия. Затем выполняется линейная РЧА вокруг устьев лёгочных вен и/или мест типичного расположения ганглионарных сплетений, с целью изоляции и модификации морфологического субстрата аритмии, в результате чего с высокой вероятностью достигается стойкий синусовый ритм и, в конечном итоге, отказ от антиаритмических препаратов и антикоагулянтов.
Опасность нелеченой ФП заключается в следующем: тромбоэмболические осложнения – инсульты, более 20% всех инсультов являются следствием ФП; дилятация камер сердца и прогрессирование сердечной недостаточности; развитие многочисленных побочных явлений от длительного приёма антиаритмических препаратов и антикоагулянтов.
В настоящее время в Клинической больнице №1 Управления делами Президента РФ, г. Москва, на базе отделения рентгенхиругических методов диагностики и лечении работает аритмологическая служба, в арсенале которой имеется самое современное оборудование и расходные материалы лучших мировых фирм-производителей, и выполняется весь спектр высокотехнологических исследований и операций при любых нарушениях ритма. Консультативный приём ведёт врач-аритмолог Мезенцев Павел Владимирович каждый понедельник с 15:00 до 18:00. Любую дополнительную информацию вы можете получить по телефону +79670466887, e-mail: .
- Comparison of Antiarrhythmic Drug Therapy and Radiofrequency Catheter Ablation in Patients With Paroxysmal Atrial Fibrillation A Randomized Controlled Trial. David J. Wilber, MD, Carlo Pappone, MD, PhD, Petr Neuzil, MD, Frank Marchlinski, MD, Andrea Natale, MD
- 2012 HRS/EHRA/ECAS Expert Consensus Statement on Catheter and Surgical Ablation of Atrial Fibrillation: Recommendations for Patient Selection, Procedural Techniques, Patient Management and Follow-up, Definitions, Endpoints, and Research Trial Design. Hugh Calkins, MD, FACC, FHRS, FAHA; Karl Heinz Kuck, MD, FESC; Riccardo Cappato, MD, FESC; Josep Brugada, MD, FESC; A. John Camm, MD, PhD; Shih-Ann Chen, MD, FHRS
Авторы: Мезенцев П. В., Ардашев В. Н.
Ресинхронизирующая терапия при хронической сердечной недостаточности.
По данным Европейского Общества Кардиологов распространённость хронической сердечной недостаточности (ХСН) в европейской популяции колеблется от 0,4 до 2%, что абсолютных цифрах составляет около 10 млн. человек.
По данным Фремингемского исследования средняя 5-летняя выживаемость во всей популяции больных с ХСН составляет 65% для мужчин и 47% для женщин, среди больных с тяжёлой ХСН, III – IV ФК по NYHA, - 35-50% в течении года.
Сегодня существуют следующие методы лечения ХСН:
- Медикаментозный;
- Электрокардиостимуляция – сердечная ресинхронизирующая терапия (СРТ);
- Хирургический: клапанная коррекция, кардиомиопластика, имплантация поддерживающих устройств.
Впервые положительный опыт в лечении ХСН у больных с дилятационной кардиомиопатией (ДКМП) с помощью электрокардиостимуляции (ЭКС) был получен Margaret Hochleitner в 1990-1992 гг., когда использовалась постоянная двухкамерная (предсердно-желудочковая) электростимуляция с укороченной атриоваентрикулярной (АВ) задержкой. В 1994 г. группы исследователей во главе с S.Cazeau и P.Bakker впервые применили трёхкамерную (атрио-бивентрикулярную) ЭКС для лечения больных с тяжёлой ХСН в сочетании с внутрижелудочковой блокадой и добились значительного улучшения их состояния.
В основе этого метода лежит ресинхронизация, коррекция электромеханических расстройств миокарда, связанных с нарушением внутри- и межжелудочкового проведения, которое имеет место и отмечается на ЭКГ расширением комплекса QRS приблизительно у 10% больных с ХСН. Это обусловлено тем, что внутри- и межжелудочковые блокады приводят к асинхронному сокращению желудочков (десинхронизации), систолической и диастолической дисфункции, митральной и трикуспидальной регургитации, что подтверждено объективными методами: трёхмерной и цвето-кинетической эхокардиографией, тканевой доплерографией, трёхмерной магниторезонансной томографией сердца. Соответственно, ресинхронизация сердца – значит электростимуляция отделов сердца, возбуждающихся с опозданием вследствие замедления проведения по системе Гиса-Пуркинье, и восстановление синхронного сокращения обоих желудочков. С этой целью пациентам с ХСН имплантируется трёхкамерный ЭКС с электродами в правое предсердие, правый желудочек, левый желудочек доступом через венозную систему сердца (коронарный синус).
В этой связи, СРТ показана больным с ХСН III-IV функционального класса, резистентной к адекватной медикаментозной терапии, фракцией выброса левого желудочка менее 35%, конечнодиастолический размер более 55 мм, шириной комплекса 120 мс и более. Кроме того, предикторами эффективности СРТ являются следующие эхокардиографические критерии: задержка предизгнания в аорте > 140 мс,, межжелудочковая механическая задержка > 40 мс, сегментарное постситолическое сокращение ЛЖ, и другие критерии.
Уже в ранние сроки после начала бивентрикулярной стимуляции почти 70% больных отмечают значительное улучшение состояния. Объективно это выражается в увеличении толерантности к физической нагрузке, уменьшении митральной и трикуспидальной регургитации, увеличении времени диастолического наполнения желудочков, снижении давления в лёгочной артерии и давления заклинивания, уменьшение конечно-диастолического и конечно-систолического объёмов левого желудочка, повышении сердечного выброса и фракции выброса, снижении в крови концентрации предсердного натрийуретического пептида. Эти данные подтверждены результатами рандомизированных многоцентровых исследований: MUSTIC (Multi-Site Stimulation in Cardiomyopathy), PATH_CHF (Pacing Therapies for Congetive Heart Failure), MIRACLE (Multi Center In Sync Randomized Clinical Trial).
В настоящее время в Клинической больнице №1 Управления делами Президента РФ, г. Москва, на базе отделения рентгенхиругических методов диагностики и лечении проводится лечение ХСН методом имплантации ресинхронизирующих устройств, а так же весь спектр диагностических и лечебных мероприятий, в т. ч и оперативное лечение, пациентов с нарушениями ритма сердца.
Консультативный приём аритмолога проводится каждые понедельник и четверг с 15:00 до 17:00 Мезенцевым Павлом Владимировичем. Любую дополнительную информацию вы можете получить по телефону 89670466887, e-mail: .
Современный подход к диагностике и лечению желудочковой экстрасистолии
Желудочковая экстрасистолия (ЖЭ) – одно из часто встречающихся нарушений ритма, связанное с повышенной электрической активностью миокарда желудочков, проявляющееся внеочередным, не связанным с синусовым, возбуждением (сокращением) сердца.
Этиология ЖЭ многофакторная, идиопатическая (не связана с какой либо органической патологией), ЖЭ на фоне органических, диспластических, склеротических, рубцовых изменений, дилатации, гипертрофии, миокарда желудочков. Пациенты с ЖЭ жалуются на перебои в работе сердца, иногда связанную с этим общую слабость головокружение и даже обмороки (синкопы). В сочетании со сниженной фракцией выброса сердца и перенесенным инфарктом миокарда, ЖЭ является предиктором внезапной смерти пациентов.
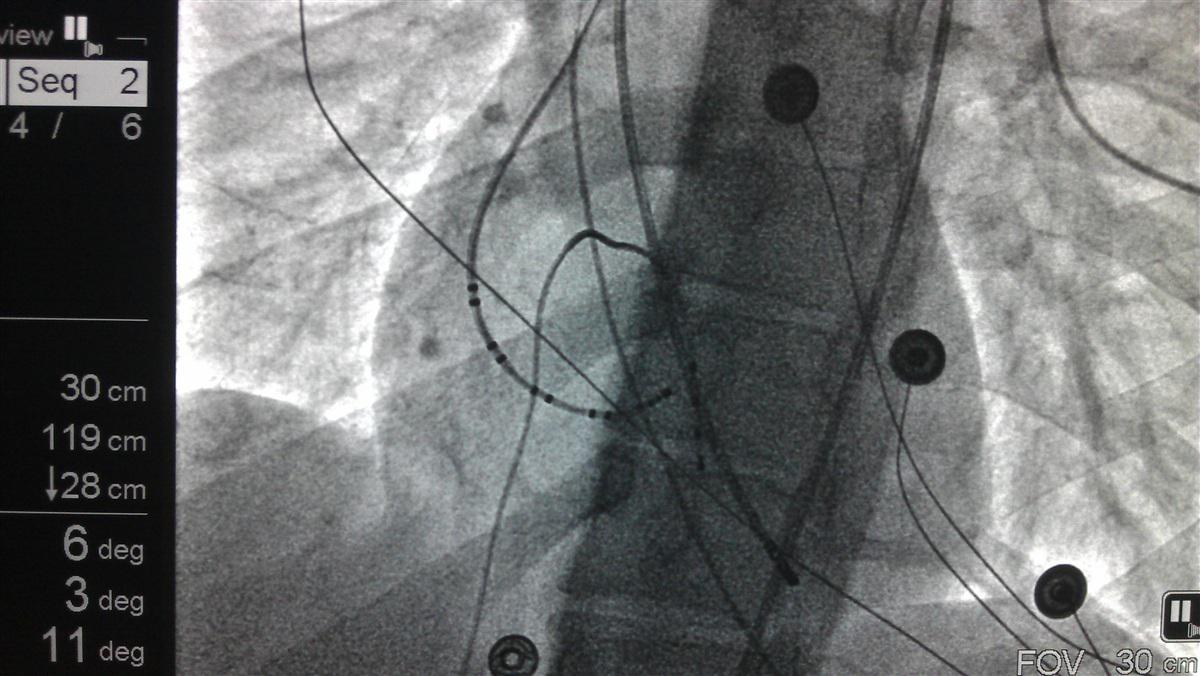
Основным методом диагностики ЖЭ является электрокардиография (ЭКГ), которая позволяет не только установить диагноз, но и с достаточно большой долей вероятности, определить локализацию эктопии, а при суточной её записи – абсолютное количество экстрасистол. Существует ряд классификаций ЖЭ, наиболее употребляемая из них, классификация B.Lown и M.Wolf (1971), по которой желудочковая экстрасистолия делится на пять градаций: 0 – отсутствие ЖЭ, 1 – редкая монотопная до 30 в час, 2 – частая монотопная более 30 в час, 3 – полиморфная ЖЭ, 4 – А спаренные ЖЭ, Б – залповые ЖЭ, пробежки желудочковой тахикардии (3 и более комплексов), 5 – ранние ЖЭ R на Т. Однако, позднее по данным некоторых исследований было установлено, что ранние экстрасистолы не несут такой большой прогностической нагрузки, и была принята исправленная классификация (B.Lown и M.Wolf (1971), в модификации M.Ryan и сотр. (1975)): отсутствие ЖЭ за 24 часа мониторного наблюдения - 0; не более 30 ЖЭ за любой час мониторирования - I; более 30 эктопических желудочковых комплексов за любой час мониторирования - II; полиморфные ЖЭ - III; мономорфные парные ЖЭ - IV-А; полиморфные парные ЖЭ - IV-Б; желудочковая тахикардия (ЖТ)- три или более подряд ЖЭ с частотой более 100 в 1 мин) – V. 3-5 функциональные классы авторами отнесены к экстрасистолии высоких градаций. Пациенты с редкой бессимптомной ЖЭ не нуждаются в антиаритмической терапии (ААТ). Частая монотопная ЖЭ (4, 5 градаций) без органической природы (идиопатическая) подлежит ААТ, при этом чаще всего используются препараты I класса по классификации Vaughan Williams E.M. 1984 (Этацизин, Пропафенон), при неэффективности III класса (d-Соталол, Амиодарон). При отсутствии эффекта от адекватной медикаментозной терапии и количестве экстрасистол 10 тысяч в сутки и более, либо при возврате ЖЭ после отмены антиаритмиков, показано оперативное лечение, катетерная радиочастотная деструкция экстрасистолического очага (рис. 1 - 3), эффективность которой составляет более 90%. ЖЭ, связанная с электролитными нарушениями (гипокалиемия), требует коррекции этих нарушений.
ЖЭ, чаще всего политопная, на фоне органических изменений в миокарде желудочков, стенозирующего атеросклероза венечных артерий, при наличии постинфарктных рубцов, хронической аневризмы сердца, выраженной гипертрофии или дилятации миокарда, требует, кроме рутинной эхокардиографии, исследования степени и характера поражения коронарного русла (коронарография), с целью определения показаний к реваскуляризации миокарда (ангиопластика и стентирование, аортокоронарное шунтирование (АКШ)), к выполнению пластических операций (аневримэктомия). Этим пациентам противопоказано назначение антиаритмических препаратов I класса, т. к. по данных многоцентровых исследований (CAST-I и CAST-II) они значительно повышают риск внезапной смерти, из-за возникновения жизнеугрожающих нарушений ритма сердца. Таким больным назначается ААТ с использованием β-адреноблокаторов (снижение смертности на 35%, Cannon D.S., Prystowsky E.N., 1999) и препаратов III класса (Амиодарон, снижение смертности более чем на 30%, исследования CAMIAT, EMIAT; или d-Соталол) с ЭКГ контролем длительности интервала QT, удлинение которого более 500 мс может привести к развитию веретенообразной желудочковой тахикардии (ЖТ) “torsades de pointes”, способную трансформироваться в фибрилляцию желудочков (ФЖ). При этом должный интервал QT определяется по формуле Базета: QTд = k х √RR, где индекс “k” у женщин равен 0.40, а у мужчин 0.37. Кроме того, пациентам, перенёсшим инфаркт миокарда, спустя 4 недели, либо через 3 месяца после АКШ, с низкой (менее 35%) фракцией выброса левого желудочка показана имплантация кардиовертера-дефибриллятора для профилактики фатальных нарушений ритма (ЖТ, ФЖ).
Таким образом, желудочковая экстрасистолия – весьма серьёзная проблема, больные, страдающие ей, нуждаются в тщательном обследовании, постоянном наблюдении, адекватной антиаритмической терапии и коррекции патологии, лежащей в основе возникновения эктопии. Все эти пациенты должны быть консультированы врачом-аритмологом.
В настоящее время в Клинической больнице №1 Управления делами Президента РФ, г. Москва, на базе отделения рентгенхиругических методов диагностики и лечении успешно работает аритмологическая служба, в арсенале которой имеется самое современное оборудование и расходные материалы лучших мировых фирм-производителей. В отделении выполняется весь спектр высокотехнологических исследований и операций при любых нарушениях ритма.
Мезенцев П. В., к.м.н. Закарян Н. В.
Рис. 1 Мужчина, 56 лет.
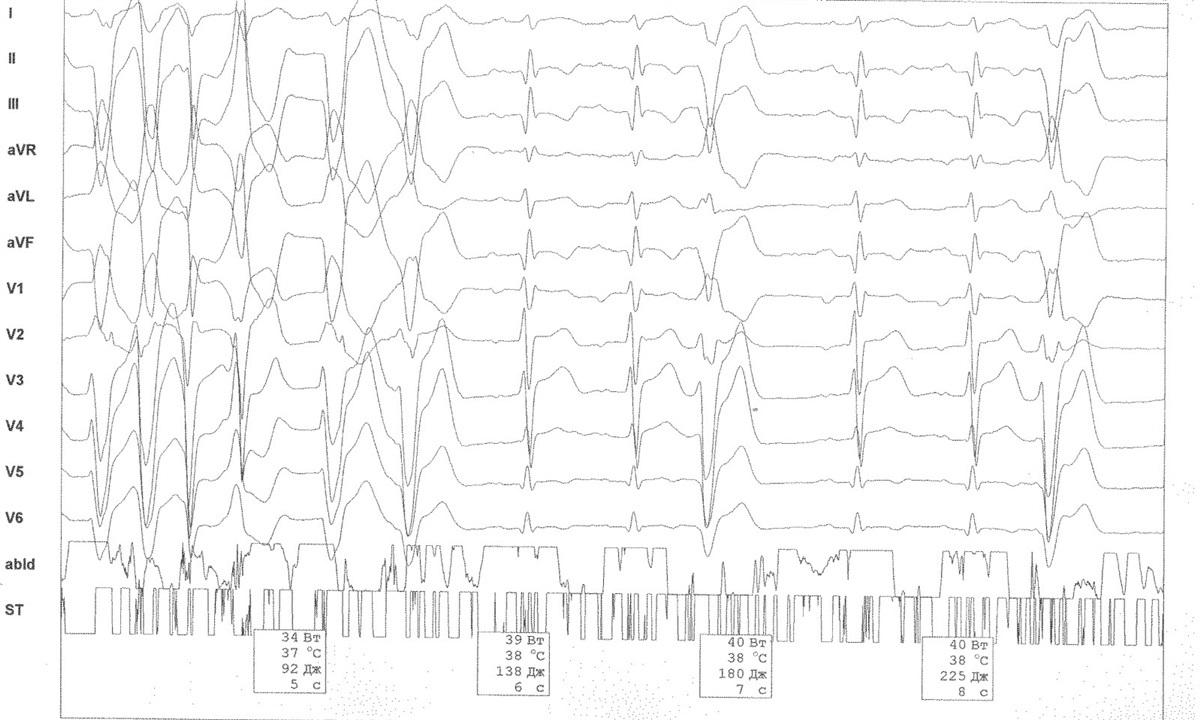
Рис. 2 Мужчина, 56 лет.
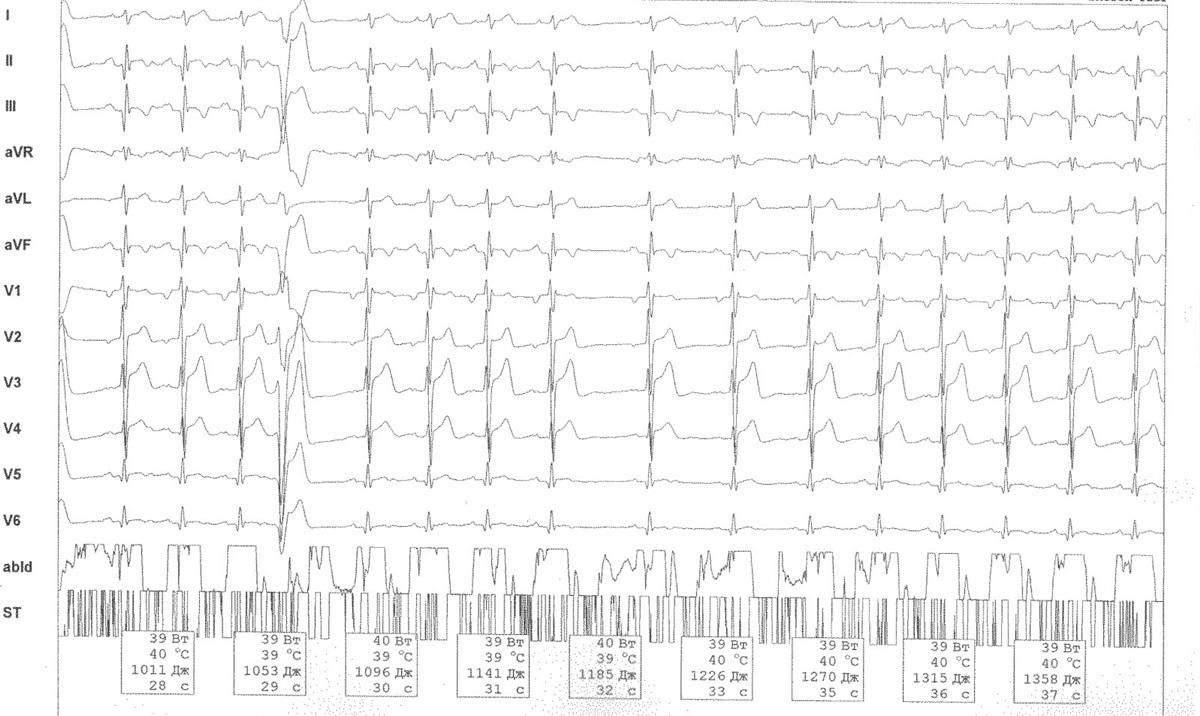
Рис. 3 Мужчина, 56 лет.